Farmacogenômica: como a genética transforma a resposta aos medicamentos
A farmacogenômica é um dos pilares da medicina personalizada moderna. Ela investiga como variações genéticas herdadas ou adquiridas influenciam a forma como cada organismo processa e responde aos medicamentos.
Na prática, isso explica por que dois pacientes podem receber a mesma droga, na mesma dose, mas apresentar efeitos completamente diferentes — desde ausência de resposta até toxicidade grave.
Ao integrar farmacologia, genética e genômica, a farmacogenômica busca escolher o medicamento certo, na dose certa, para o paciente certo, reduzindo a necessidade de decisões baseadas em tentativa e erro.
[lwptoc colorScheme="inherit" borderColor="#ffffff"]
Por que a genética influencia a resposta aos medicamentos?
A resposta a um fármaco depende de múltiplos fatores biológicos. Entre os mais importantes estão:
Variação genética e resposta a medicamentos
Pequenas alterações no DNA, como polimorfismos de nucleotídeo único (SNPs), podem modificar a eficácia, toxicidade e duração do efeito de um medicamento. Essas variações determinam, por exemplo, se um paciente metaboliza um fármaco muito rápido, muito devagar ou de forma intermediária.

Farmacocinética e farmacodinâmica
As variantes genéticas podem alterar:
Farmacocinética: absorção, distribuição, metabolismo e eliminação;
Farmacodinâmica: interação entre o medicamento e seus alvos moleculares (receptores, canais, enzimas).
Com isso, mesmo um fármaco eficaz pode falhar em pacientes cujo perfil genético modifica seu comportamento no organismo.
Genes farmacogenéticos (farmacogenes)
Os genes mais estudados incluem:
- Enzimas metabolizadoras, como CYP2D6 e CYP2C19;
- Transportadores, como SLCO1B1;
- Alvos farmacológicos, como receptores e enzimas específicas.
Eles permitem classificar pacientes como metabolizadores lentos, intermediários normais ou ultrarrápidos. Essa classificação orienta ajustes de dose e, muitas vezes, a escolha de outra droga.
Biomarcadores genéticos
A identificação de variantes associadas a risco de efeitos adversos ou falha terapêutica já faz parte das bulas de diversos medicamentos aprovados pelo FDA. Esses biomarcadores orientam condutas clínicas baseadas em evidências.

Testes farmacogenômicos: da teoria à prática clínica
A incorporação dos testes genéticos à prática médica pode ocorrer de duas maneiras:
Testes preemptivos: realizados antes do início de um tratamento, ficam incorporados ao prontuário eletrônico e podem orientar várias prescrições ao longo da vida.
Testes reativos: solicitados diante de suspeita de toxicidade, falha terapêutica ou necessidade de ajustar dose individualmente.
Sociedades internacionais como o CPIC (Clinical Pharmacogenomics Implementation Consortium) e a American Heart Association publicam recomendações para interpretar e aplicar esses testes.
Farmacogenética e Farmacogenômica: semelhanças, diferenças e evolução histórica
A farmacogenética surgiu a partir de estudos que investigavam como mutações específicas em genes individuais influenciavam a resposta a determinados medicamentos.
Esses primeiros trabalhos, ainda pontuais e focados em variantes de grande impacto clínico, levaram o médico alemão Friedrich Vogel a cunhar o termo “pharmacogenetics” em 1959.
Com o avanço das tecnologias de biologia molecular e o surgimento da genômica, o campo se expandiu significativamente, dando origem ao termo farmacogenômica, alinhado a outras áreas “ômicas” por seu foco mais amplo e sistêmico.

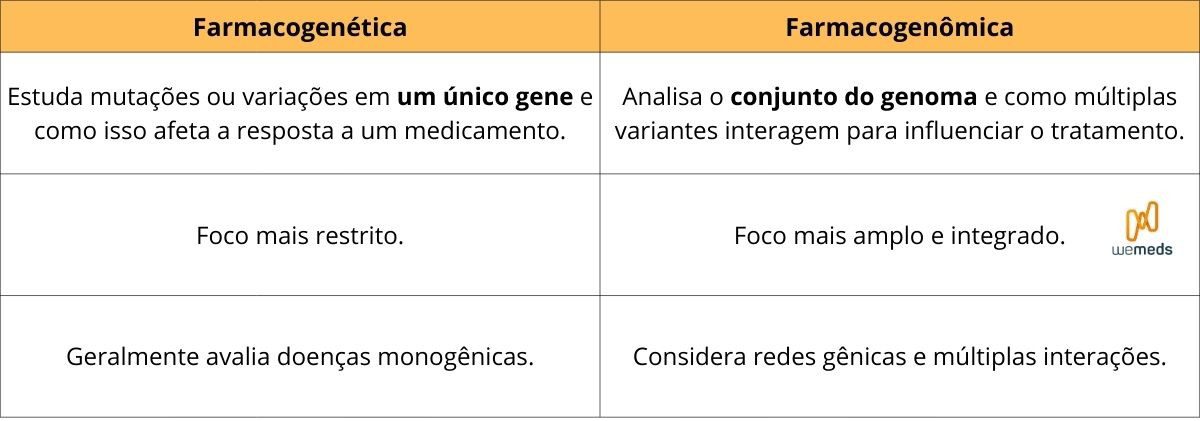
Diferença fundamental entre farmacogenética e farmacogenômica
Embora frequentemente utilizados como sinônimos, os termos representam abordagens distintas dentro do estudo da influência genética sobre a resposta a medicamentos.
Farmacogenética: enfoca variantes em genes individuais que modificam a eficácia ou toxicidade de um fármaco.
Tradicionalmente estuda polimorfismos com grande efeito funcional, como aqueles presentes nos genes CYP2D6, TPMT, NAT2, entre outros. Historicamente, buscou explicar diferenças interindividuais na resposta a medicamentos por meio da análise de um ou poucos genes.
Farmacogenômica: abrange uma visão mais integrada e abrangente, analisando múltiplas variantes genéticas simultaneamente.
Utiliza tecnologias como sequenciamento de nova geração (NGS) e estudos de associação genômica ampla (GWAS) para mapear interações complexas entre genes e vias metabólicas.
Ainda, integra outras áreas “ômicas”, como transcriptômica, proteômica e metabolômica, visando identificar biomarcadores, prever respostas terapêuticas e fundamentar estratégias de medicina personalizada.
Em resumo, enquanto a farmacogenética foca o gene, a farmacogenômica foca o genoma. Ambas contribuem de forma complementar para o desenvolvimento de terapias mais seguras, eficazes e individualizadas.
Exemplos clínicos: farmacogenômica na oncologia
A oncologia é uma das áreas que mais se beneficia dessa abordagem. Alguns exemplos importantes incluem:
Irinotecano no câncer colorretal — gene UGT1A1.
Pacientes com variantes que reduzem a atividade da enzima UGT1A1 acumulam níveis tóxicos de irinotecano, motivo pelo qual o teste UGT1A1*28 é recomendado. Nesses casos, a conduta consiste em reduzir a dose para prevenir neutropenia grave e diarreia severa, mantendo eficácia terapêutica com maior segurança.
Leucemia Linfoide Aguda em crianças — gene TPMT.
Cerca de 10% das crianças possuem variantes que diminuem a atividade da enzima TPMT, responsável pelo metabolismo das tiopurinas, o que aumenta o risco de mielotoxicidade potencialmente fatal. Por isso, a conduta recomendada é ajustar a dose de quimioterapia para reduzir a toxicidade.
Fluorouracil (5-FU) — gene DPYD.
Pacientes com deficiência parcial ou total da enzima DPD (diidropirimidina-desidrogenase) apresentam risco elevado de toxicidade grave ao 5-FU. Dessa forma, recomenda-se testar variantes do gene DPYD e, conforme o resultado, reduzir a dose ou evitar o uso do medicamento.

Esses exemplos mostram como a farmacogenômica salva vidas ao prevenir eventos adversos e aumenta a eficácia dos tratamentos.
Benefícios da farmacogenômica na prática clínica
Mais segurança: reações adversas a medicamentos são causa frequente de internação. A farmacogenômica ajuda a identificar quem está mais vulnerável.
Terapias mais eficazes: a escolha personalizada do fármaco aumenta a chance de resposta clínica positiva.
Redução de custos: evita tratamentos ineficazes, diminui complicações e reduz hospitalizações.
Menos tentativa e erro: a análise genética permite decisões fundamentadas antes do início do tratamento.
Desafios e limitações atuais
Apesar do avanço, a incorporação ampla da farmacogenômica enfrenta obstáculos:
- Alto custo dos testes e cobertura limitada pelos planos de saúde.
- Baixa disponibilidade tecnológica em muitos centros.
- Dificuldades de implementação, como integração com prontuários eletrônicos.
- Falta de validação em populações geneticamente diversas, especialmente na América Latina.
- Barreiras educacionais entre profissionais de saúde.
- Questões éticas e de privacidade relacionadas ao uso de dados genéticos.
Superar esses desafios é fundamental para expandir o acesso à medicina de precisão.

Conclusão: o futuro da prescrição é personalizado
A farmacogenômica está transformando a forma como escolhemos, ajustamos e monitoramos medicamentos. Ao reconhecer que cada paciente possui um perfil genético único, essa área permite maximizar o benefício terapêutico, minimizar riscos e promover um cuidado muito mais eficiente e personalizado.
À medida que os testes farmacogenéticos se tornam mais acessíveis e as diretrizes clínicas mais disseminadas, a farmacogenômica deve ocupar um papel central na rotina médica — inclusive no Brasil.
Leia também: Medicina de Precisão, Bioética e Farmacogenômica: experiência centrada no indivíduo
Referências:
Sadee, W., Wang, D., Hartmann, K., & Toland, A. E. (2023). Pharmacogenomics: Driving Personalized Medicine. Pharmacological reviews, 75(4), 789–814. https://doi.org/10.1124/pharmrev.122.000810
Roden, D. M., McLeod, H. L., Relling, M. V., Williams, M. S., Mensah, G. A., Peterson, J. F., & Van Driest, S. L. (2019). Pharmacogenomics. Lancet (London, England), 394(10197), 521–532. https://doi.org/10.1016/S0140-6736(19)31276-0
Cecchin, E., & Stocco, G. (2020). Pharmacogenomics and Personalized Medicine. Genes, 11(6), 679. https://doi.org/10.3390/genes11060679
Guolin Wen, A., Wen, S., & Patel, P. (2025). Pharmacogenomics Overview. In StatPearls. StatPearls Publishing.
Weinshilboum, R. M., & Wang, L. (2006). Pharmacogenetics and pharmacogenomics: development, science, and translation. Annual review of genomics and human genetics, 7, 223–245. https://doi.org/10.1146/annurev.genom.6.080604.162315
Auwerx, C., Sadler, M. C., Reymond, A., & Kutalik, Z. (2022). From pharmacogenetics to pharmaco-omics: Milestones and future directions. HGG advances, 3(2), 100100. https://doi.org/10.1016/j.xhgg.2022.100100