Doação de sangue universal: a enzima que pode revolucionar a medicina transfusional
[lwptoc colorScheme="inherit" borderColor="#fcfcfc"]
Sangue universal: menos de 10% da população tem sangue O-
Você já parou para pensar que, em uma emergência, o tempo gasto para identificar o tipo sanguíneo pode ser decisivo? Agora imagine se toda doação pudesse ser usada em qualquer paciente, sem risco de incompatibilidade. Parece ficção científica, mas a ciência está cada vez mais perto de tornar isso realidade.
A transfusão de sangue é um dos pilares da medicina moderna. A escassez de bolsas de sangue do tipo O negativo — apenas 8 a 9% da população mundial — gera gargalos logísticos e aumenta o risco em situações de emergência.
Desde as primeiras tentativas no século XVII até a descoberta dos grupos sanguíneos por Karl Landsteiner, em 1901, aprendemos que compatibilidade é questão de vida ou morte. O sistema ABO, com suas diferenças de antígenos na superfície das hemácias, sempre foi um desafio logístico: manter estoques de todos os tipos sanguíneos, prever demandas e evitar desperdícios.
Mas, e se todo sangue pudesse ser transformado em O universal?
Sangue universal: a tecnologia por trás da ideia
Um estudo recente publicado na Nature Biomedical Engineering apresenta uma abordagem inovadora: o uso de enzimas específicas capazes de remover os antígenos A e B das hemácias humanas, convertendo-as em células do tipo O - o sangue universal. Essa técnica já vinha sendo explorada em modelos experimentais, mas agora alcançou um nível de eficiência e segurança que permite vislumbrar aplicações clínicas.
Segundo a reportagem do Medical Xpress, a equipe responsável conseguiu otimizar enzimas derivadas de bactérias intestinais, tornando-as mais seletivas e eficazes. O resultado: glóbulos vermelhos “limpos”, sem os marcadores que desencadeiam reações imunológicas em receptores incompatíveis.

Mecanismo bioquímico
- As enzimas utilizadas são glicosidases bacterianas otimizadas por engenharia de proteínas.
- Elas atuam removendo os resíduos de açúcares específicos (N-acetilgalactosamina no tipo A e galactose no tipo B) presentes na superfície das hemácias.
- O resultado é a eliminação dos epítopos antigênicos responsáveis pela resposta imune mediada por anticorpos anti-A e anti-B.
Esse processo preserva a integridade estrutural e funcional da membrana eritrocitária, mantendo a viabilidade celular para transfusão.
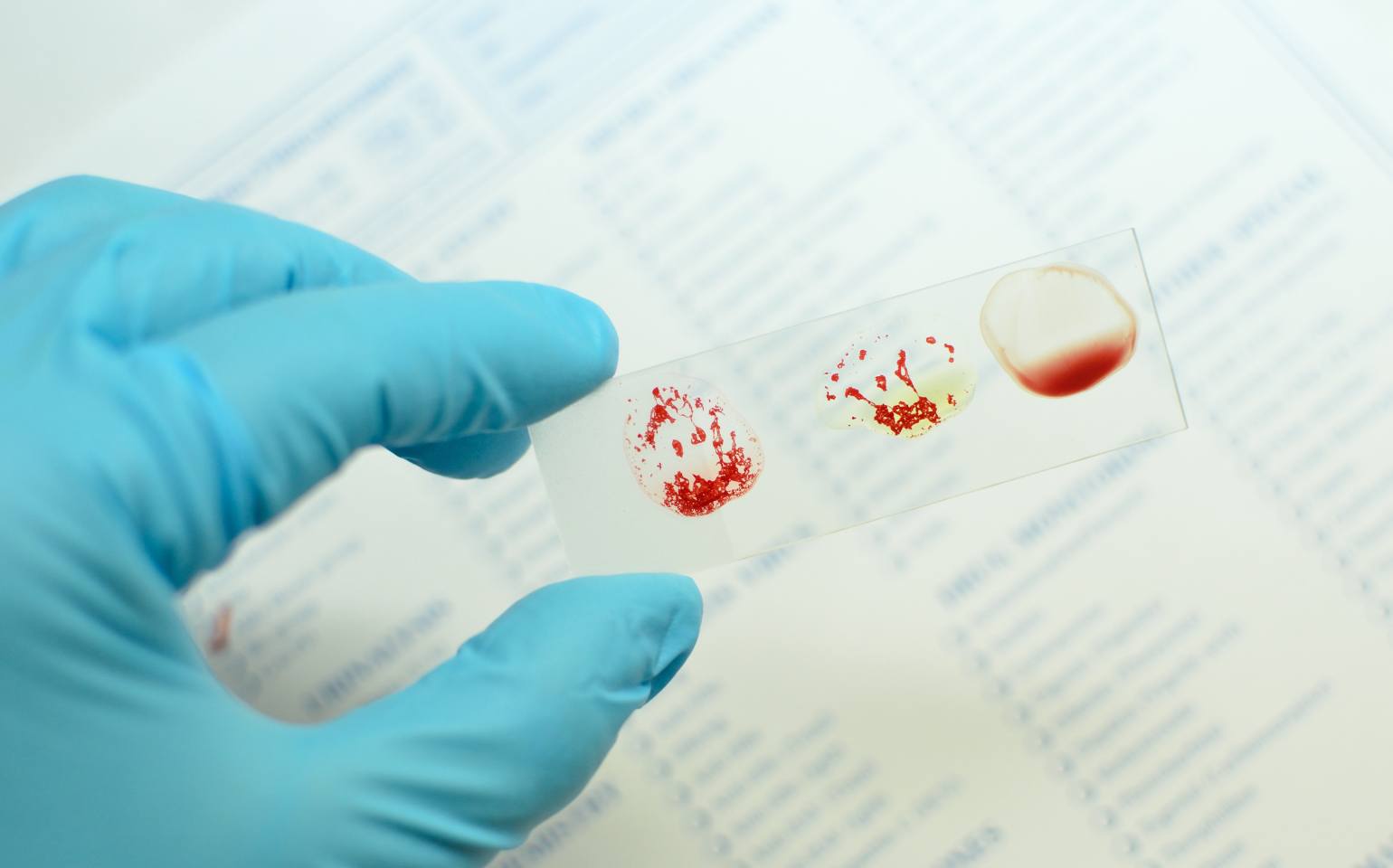
Metodologia do estudo
Para criar o sangue universal, os pesquisadores utilizaram enzimas glicosidases derivadas de bactérias intestinais (principalmente Flavonifractor plautii), otimizadas por engenharia de proteínas para maior seletividade.
Processo experimental:
- Hemácias humanas dos tipos A e B foram incubadas em solução contendo as enzimas modificadas.
- O tempo médio de reação foi de 60 a 120 minutos, em condições controladas de pH e temperatura.
- Após o tratamento, as células foram lavadas e submetidas a testes de aglutinação e citometria de fluxo.
Resultados quantitativos:
- Redução de >99,9% dos resíduos antigênicos A e B detectáveis.
- Em ensaios de aglutinação, as hemácias convertidas não reagiram com soros contendo anticorpos anti-A ou anti-B.
- A viabilidade celular permaneceu acima de 95%, sem alterações significativas na morfologia eritrocitária.
- Em modelos pré-clínicos, não foram observadas reações hemolíticas imediatas.

Achados principais
- A conversão foi altamente eficiente em diferentes amostras de sangue, sugerindo aplicabilidade ampla.
- O processo não comprometeu a integridade da membrana eritrocitária nem a capacidade de transporte de oxigênio.
- A técnica mostrou potencial de escalabilidade, com custo estimado competitivo frente ao desperdício atual de bolsas incompatíveis.
Impacto clínico e logístico
Se essa tecnologia se consolidar, os bancos de sangue poderão:
- Reduzir drasticamente a escassez de tipos sanguíneos raros.
- Simplificar a logística de armazenamento e distribuição, com estoques unificados, reduzindo perdas por vencimento.
- Aumentar a segurança transfusional, já que o risco de incompatibilidade e reações hemolíticas agudas seria minimizado.
- Impacto em emergências, permitindo transfusões imediatas sem tipagem prévia, especialmente em politraumas e hemorragias massivas.
💡 Imagine um pronto-socorro em que cada bolsa disponível pudesse ser usada em qualquer paciente, sem a corrida contra o tempo para tipagem e compatibilidade, com estoque mais simples, menos desperdício e mais segurança.
Limites e desafios para medicina transfusional
Apesar do entusiasmo, ainda há pontos críticos:
- Segurança imunológica: comprovar ausência de resíduos antigênicos detectáveis por anticorpos naturais.
- Custo e escalabilidade: transformar milhões de bolsas de sangue exige processos industriais robustos.
- Regulação: aprovação por agências como FDA e EMA dependerá de ensaios clínicos robustos, avaliando eficácia e segurança a longo prazo.
- Compatibilidade além do ABO: o fator Rh e outros sistemas menores (Kell, Duffy, Kidd) continuam sendo relevantes.

O futuro da transfusão
A conversão enzimática de hemácias representa um marco potencial na medicina transfusional. Se validada em estudos clínicos multicêntricos, poderá transformar a gestão de hemocentros, reduzir desigualdades no acesso ao sangue e aumentar a segurança transfusional globalmente.
Mais do que uma inovação laboratorial, trata-se de uma mudança de paradigma: a possibilidade de tornar cada doação um recurso universal, ampliando a autonomia dos sistemas de saúde e salvando vidas em contextos críticos.
Estaremos diante do fim da tipagem sanguínea como conhecemos?
--
Referências:
Medical Xpress. “Enzyme technology could make human blood universally compatible.” (2025). https://medicalxpress.com/news/2025-10-enzyme-technology-human-universal-donor.html
MacMillan, S., Hosgood, S.A., Walker-Panse, L. et al. Enzymatic conversion of human blood group A kidneys to universal blood group O. Nat Commun 15, 2795 (2024). https://doi.org/10.1038/s41467-024-47131-9